2 Diagnostika a léčba onemocnění žlučníku
2.1 Úvod
Cholecystektomie patří k nejčastějším operacím na chirurgických pracovištích. Počítá se k výkonům středně obtížným a od roku 1892, kdy ji Langenbuch provedl poprvé, se na technice prakticky nic nezměnilo. Po 100 letech v roce 1987 prof. Mouret v Lyonu ve Francii zahájil laparoskopickou cholecystektomií revoluci v technice operování. Právě cholecystektomie se ukázala jako nejvhodnější operace k prosazení laparoskopické metody.
Dnes všeobecně uznávané výhody laparoskopické operace – méně bolesti po operaci, rychlejší rekonvalescence, kratší hospitalizace, lepší kosmetický efekt – přiváděly z počátku pacienty na ta pracoviště, která s touto metodou začala. Prudký úbytek cholecystektomií na chirurgiích, kde neměli laparoskopickou aparaturu, pak přesvědčil všechny chirurgy, že bez laparoskopického operování se nelze obejít.První laparoskopická operace v českých zemích, laparoskopická cholecystektomie, byla provedena českými chirurgy dne 20. září 1991 v Českých Budějovicích.
2.2 Klinický obraz a diagnostika cholelitiázy
Cholecystolitiáza má v podstatě dvě příznakové formy: 1. forma dyspeptická,2. forma koliková.
- Forma dyspeptická – je provázena souborem nespecifických příznaků – nepříjemný a bolestivý tlak v nadbřišku, spíše v pravém podžebří. Dále nauzea, zvracení, nadýmání,… Klinicky se projevuje bolestivostí v pravém podžebří při palpaci. Typický je příznak Murphyho – bolestivá reakce pacientapři palpaci pod pravým obloukem žeberním při současném nadechnutí.
- Forma koliková – žlučové koliky. Kolikovité bolesti mohou být vyprovokovány jídlem, stresem, převážně je příčinou uzávěr cystiku kamenem. Projevují se křečovitými bolestmi v pravém podžebří často vystřelující do pravého ramenního kloubu.
Obě tyto formy cholelitiázy se mohou komplikovat a měnit klinický obraz. Jednou z komplikací je zánět, od prosté cholecystitidy po empyém žlučníku, pericholecystický infiltrát, a dokonce perforaci žlučníku s biliární peritonitidou. Další komplikací může být ikterus – konkrement v choledochu nebo útlak žlučových cest například zánětlivým infiltrátem. Zánět může pokračovat na žlučové cesty s typickou cholangoitidou – vysoké teploty, třesavky.
Diagnostika cholecystolitiázy musí být ze strany lékaře velmi aktivní. Základní diagnostickou metodou je sonografické vyšetření dutiny břišní, prostý rtg snímek břicha a komplexní laboratorní vyšetření. Všechny tyto metody provádíme vždy u každé náhlé příhody břišní.
Důvod je prostý – jedna třetina pacientů má cholecystolitiázu, ale to ještě neznamená, že cholecystolitiáza je příčinou potíží pacienta. Podrobnější rozbor diagnostických metod viz kapitola Indikace.
2.3 Indikace a kontraindikace operace
K laparoskopické cholec ystektomii indikujeme symptomatickou cholecystolitiázu na podkladě laboratorního vyšetření a sonografického vyšetření žlučníku a žlučových cest. Indikace se prakticky neliší od indikace k otevřené cholecystektomii. U sonografického vyšetření vyžadujeme popis šíře stěny žlučníku, obsahu žlučníku, jeho velikost a dále šíři choledochu. Tam, kde je šíře choledochu větší než 8 mm, je nález suspektní z choledocholitiázy a indikujeme endoskopickou retrográdní cholangiopan kreatografii (ERCP) s eventuální extrakcí konkrementů.
O úloze ERCP v léčbě choledocholitiázy se zmíníme ještě dále. Dnes můžeme říci, že 95% pacientů se symptomatickou cholecystolitiázou může být indikováno k laparoskopické cholecystektomii. Původně stanovená kritéria relativních kontraindikací – svraštělý žlučník, obezita, silnější stěna žlučníku než 7 mm, srůsty po předchozích operacích v nadbřišku – dnes již všeobecně neplatí.
Záleží na technickém vybavení pracoviště, na vyspělosti operatéra, co považuje ještě za indikaci a co za kontraindikaci k laparoskopické cholecystektomii.
Laparoskopická cholecystektomie se provádí i v těhotenství. Laparoskopickou cholecystektomii mohou podstoupit pacienti s akutní cholecystitidou a enormně obézní. Cholecystoenterální píštěl může být rovněž vyřešena laparoskopicky při znalosti práce s endostaplery a endostehem.
Absolutní kontraindikace k laparoskopické cholecystektomii prakticky není, vždy je třeba pacienta posuzovat individuálně ve spolupráci s anesteziologem.
2.4 Laparoskopická cholecystektomie
2.4.1 Technika operace
Uložení pacienta
V zásadě existují dva způsoby operace:
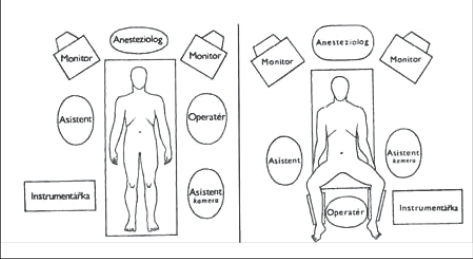
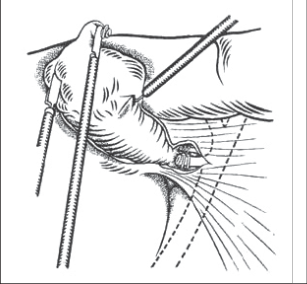
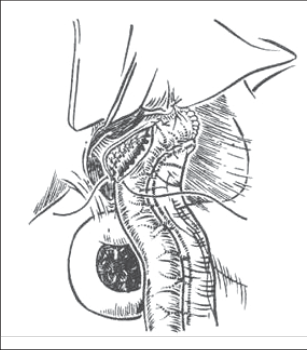
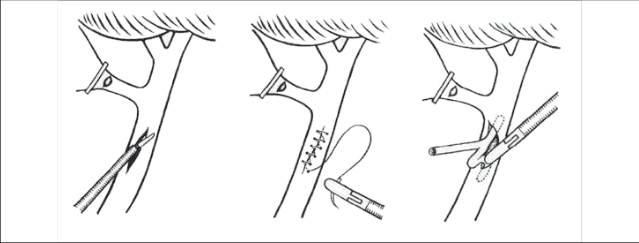
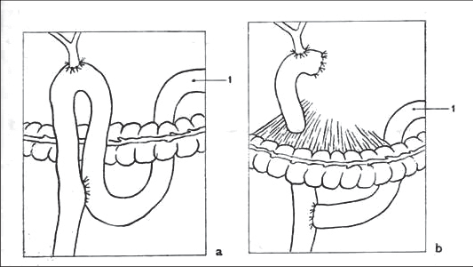
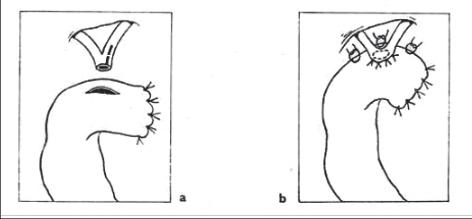
- Způsob „americký“, kdy pacient leží na zádech, operatér stojí vlevo od pacienta, „ asistent-kameraman“ po jeho levé ruce a další asistence naproti operatéra. Instrumentářka stojí vpravo od dolních končetin operovaného, dva monitor y jsou pak po stranách hlavy pacienta. Tato metoda umožňuje operatérovi pracovat jen s jedním nástrojem, což je výhodné pro období, kdy chirurg s laparoskopickými operacemi začíná. Asistence pak přidržuje žlučník za fundus a infundibulum žlučníku. I u tohoto způsobu však operatér může pracovat obouruč, což umožňuje mnohem jemnější techniku operování (obr. 1a).
- Způsob „francouzský“, kdy pacient leží na zádech s abdukovanými dolními končetinami, operatér pak stojí mezi nohama pacienta a operuje obouručnou technikou. Asistence držící kameru stojí na levé straně operačního stolu, asistence držící fundus žlučníku stojí na pravé straně operačního stolu (obr. 1b).
Dnes se jednoznačně operuje obouručně stejně jako u klasické operace. Asistent je jen jeden, nebo dokonce chirurg operuje sám s instrumentářkou.
Zavedení trokarů
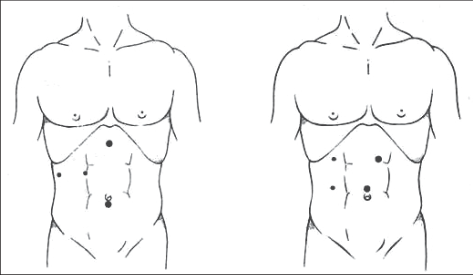
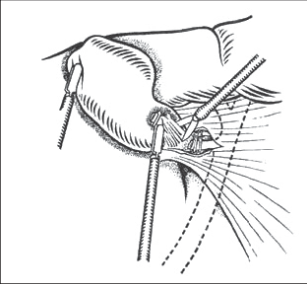
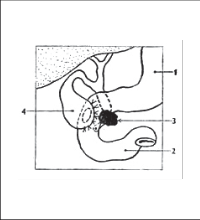
Obvyklé umístění trokarů je ukázáno na obrázcích níže (obr. 2). Zavádění trokarů závisí na zvyklostech pracoviště. Nejprve vedeme drobnou kožní incizi pod nebo nad pupkem v délce asi 10 mm. Po vyzvednutí stěny břišní za kožní řasu kolmo zavádíme Veressovou jehlu do dutiny břišní. Po dosažení nastaveného nitrobřišního tlaku CO2 na 11–12 mm Hb zavádíme stejnou incizí 10mm trokar pro optiku s videokamerou. Sami u laparoskopické cholecystektomie používáme kovových trokarů. První trokar zavádíme v oblasti pupku „naslepo“ šikmo proti bránici a po „napíchnutí“ vyzvedneme trokarem stěnu břišní a pronikáme tlakem na trokar dále do dutiny břišní, neprocházíme tedy kolmo stěnou břišní. Na zavádění tohoto trokaru se podílejí obě ruce operatéra, pravá ruka udržuje směr zavádění a slouží také jako „zarážka“ při proniknutí stěnou. Pokud používáme plastický trokar s pružným krytem, musíme procházet stěnou břišní kolmo. Při tzv. otevřené technice zavedení trokarů postupně incidujeme všechny vrstvy stěny břišní včetně peritonea a zavádíme trokar s tupým mandrénem. Místo incize kolem trokaru utěsňujeme stehem. Pak připojujeme hadičku insuflace a zavádíme buď rovnou, nebo šikmou optiku (preferujeme šikmou).Po přehlédnutí dutiny břišní za optické kontroly zavádíme hlavní pracovní trokar asi 2cm pod processus xiphoideus (10 mm), vždy vpravo od ligamentum teres hepatis. Dva 5mm trokary pak zavádíme v pravém podžebří, jeden těsně pod obloukem v přední axilárně čáře, druhý v čáře medioklavikulární v úrovni poloviny vzdálenosti mezi pupkem a žeberním obloukem. Tyto dva 5mm trokary slouží k zavedení nástrojů, k držení a manipulaci se žlučníkem. Po zavedení trokarů upravujeme polohu nemocného s operačním stolem do anti-Trendelenburgovy polohy (asi 20 st.) a nakláníme asi 15 st. doleva. Touto polohou kličky střevní uvolní subhepatální prostor. Zavedení trokarů je vždy individuální dle potřeby – není nutné dodržovat výše uvedený postup.
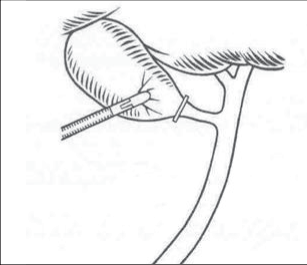
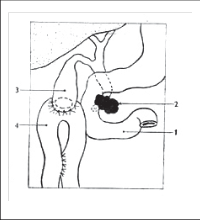
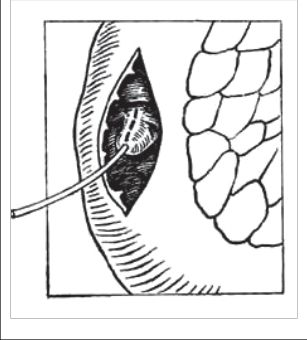
Kleštěmi zavedenými trokarem v přední čáře axilární držíme fundus žlučníku, kleštěmi zavedenými trokarem v čáře medioklavikulární pak držíme infundibulum žlučníku (obr. 3).
Operatér drží levou rukou infundibulum a manipuluje s krčkem žlučníku tak, jak potřebuje. Hlavním pracovním trokarem pod processus xiphoideus zavádíme operační nástroje, operační kleště, nůžky, koagulační háček, eventuálně sací a výplachovou kanylu, ultrasonografické nástroje.
Uvolnění žlučníku
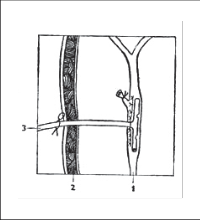
Fundus žlučníku mobilizujeme směrem ventrálním a kraniálním, tím zpřehledňujeme oblast Calotova trojúhelníku. Pokud jsou v oblasti žlučníku adheze, nejčastěji omenta se stěnou žlučníku, tyto rozrušujeme. Je-li stěna žlučníku napjatá a nelze ji uchopit do kleští – hydrops nebo empyém, provádíme punkci žlučníku. Silnou jehlu zavádíme samotným vpichem přes stěnu břišní pod pravým žeberním obloukem a do lumen žlučníku pronikáme v oblasti fundu. Po dokončení punkce a odstranění jehly uzavíráme punkční otvor branžemi úchopových kleští.
Preparace v Calotově trojúhelníku
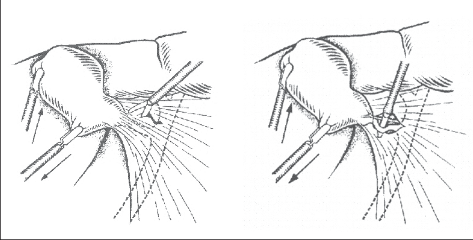
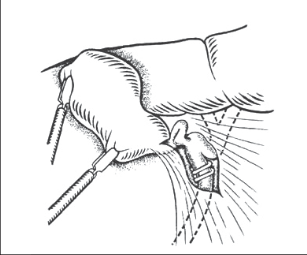
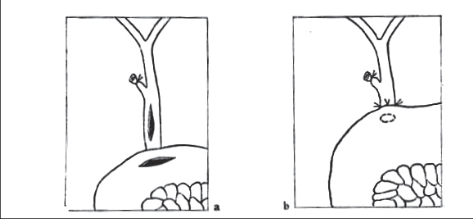
Pomocí háčkové elektrody nebo preparačních nůžek izolujeme ductus cysticus, začínáme vždy u krčku žlučníku (obr. 4a).
Používáme-li k preparaci háčkové elektrody, snažíme se vyvarovat koagulace pro možné tepelné poranění společného žlučovodu. Sami jsme užívali k této preparaci háčkové elektrody. Později jsme přešli v této oblasti na preparaci pomocí nůžek, neboť se nám zdá, že práce s nimi je jemnější a přesnější. Dnes se s oblibou používají sonografické nástroje, které riziko tepelného poranění snižují na minimum. Při preparaci v Calotově trojúhelníku je výhodné kleštěmi držícími infundibulum žlučníku manipulovat touto částí zleva doprava a naopak, což nám umožní lepší expozici duktus cysticus.Pomocí preparačních nůžek nebo háčkové elektrody obcházíme duktus cysticus, abychom získali dostatečný prostor k naložení klipů. Zde je důležité vidět, že ductus cysticus navazuje na krček žlučníku, aby nedošlo k záměně duktus cysticus za duktus choledochus.
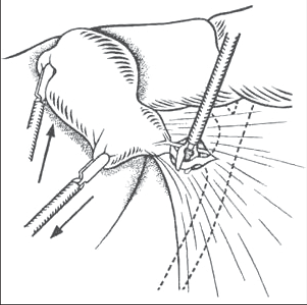
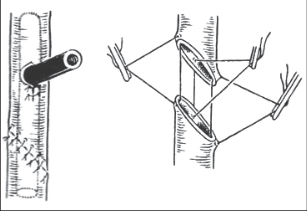
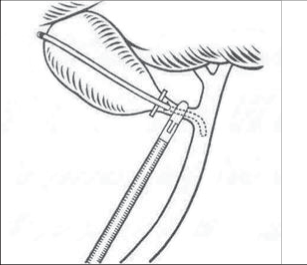
Pokud jsou v této oblasti těžké zánětlivé změny, můžeme naopak preparovat duktus cysticus centrálně až k junkci ductus hepaticus, abychom měli jistotu, že neizolujeme společný žlučovod. Někdy je tato fáze operace velmi jednoduchá, jindy velmi složitá. Ductus cysticus klipujeme dvěma klipy centrálně blíže choledochu a jedním klipem periferně (obr. 4b).Pak jej přerušujeme nůžkami. Kleště přemísťujeme z infundibula žlučníku na volnou přerušenou část ductus cysticus a stejným způsobem pak preparujeme arteria cystica. Centrálně tepnu uzavíráme dvěma klipy a přerušujeme ji. Izolace žlučníku z lůžka se provádí háčkovou elektrodou nebo preparačními nůžkami za pečlivého stavění krvácení (obr. 5 a 6).
Ošetření lůžka žlučníku
Po uvolnění celého žlučníku z lůžka jej přemísťujeme nad konvexitu jater, kleštěmi vyzvedáváme jaterní okraj, lůžko žlučníku oplachujeme a znovu kontrolujeme, zda nedochází ke krvácení. Krvácení z drobnějších cév stavíme háčkovou elektrodou, z větších cév pak koagulací po předchozím zachycení do branží disektoru. Jestliže se jedná o plošné krvácení, můžeme přiložit lokální hemostyptika – Spongostan, Gelaspon, Surgicell. Při kontrole lůžka musíme počítat i s možným aberantním žlučovodem.
Drobný aberantní žlučovod můžeme uzavřít koagulací, větší pak naložením klipů. Koagula odstraňujeme jednak pomocí sací kanyly, pevná koagula je možné odstranit pomocí 10mm extrakčních kleští.
Zavedení drénu
Na našem pracovišti se provádí rutinně drenáž, zavádíme drén 5mm trokarem umístěným v přední axiální čáře do subhepatálního prostoru. Samotný trokar pak odstraňujeme a drén fixujeme stehem.
Extrakce žlučníku
V další fázi operace přemísťujeme laparoskop do trokaru pod processus xiphoideus a do trokaru u pupku zavádíme extrakční kleště. Jimi zachycujeme igelitový sáček se žlučníkem. Podle velikosti žlučníku pak skalpelem rozšiřujeme incizi pod pupkem a extrahujeme sáček se žlučníkem současně i s trokarem z dutiny břišní. Tuto incizi u pupku uzavíráme většinou dvěma stehy naloženými na fascii. Po odstranění zbylých trokarů je pak provedena sutura podkoží a kůže.
Preparát
Bezprostředně po operaci operatér prohlédne preparát a rozstřihne žlučník včetně ductus cysticus. Může tak posoudit sílu stěny žlučníku, obsah žlučníku a hlavně při určitých pochybnostech posoudit oblast ductus cysticus, zda neobsahuje i resekovanou část ductus choledochus. Pokud je vyťata přilehlá část choledochu, je to na preparátu vždy vidět. Je zde ještě poslední příležitost provést časnou revizi, aniž pacient dosud opustil operační sál.
2.4.2 Peroperační biligrafie
Cholechodocholitiáza se dnes většinou řeší endoskopickou cestou. Tam, kde je předoperační podezření na obstrukci, provádíme ERCP. Tato je možná i u prokázaných alergií na kontrastní látku, nejde o parenterální podání kontrastu, je použitelná i u vyšších hodnot bilirubinu a umožňuje v jednom sezení terapii, tzn. endoskopickou papilosfinkterotomii a extrakci kamenů. Pak již následuje jen laparoskopická cholecystektomie. Vzhledem k nízké incidenci (3,5%) tzv. němé choledocholitiázy se nedoporučuje provádět ERCP paušálně.
Předoperační biligrafie, jak uvádějí někteří autoři, se všeobecně neujala a je obsoletní metodou. Peroperační biligrafie napomáhá definování anatomických poměrů extrahepatálního řečiště, např. při podezření na poranění nebo na choledocholitiázu, kdy sonografický předoperační nález neodpovídá operačnímu nálezu.
Technika provedení peroperační biligrafie
V podstatě jsou dvě možnosti náplně žlučových cest:
- punkční – nabodnutím žlučníku,
- transcystická biligrafie.
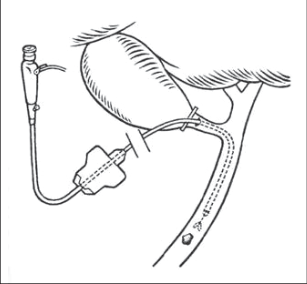
Nejčastěji je používána metoda transcystická. Po vypreparování ductus cysticus v dostatečné délce tento uzavřeme vysoko pod infundibulem klipem. Ductus cysticus nastřihneme, disektorem dilatujeme lumen, do kterého pak zavádíme katétr s kovovým vodičem. Centrální část ductus cysticus s katétrem pak uzavíráme neúplně dovřeným klipem. Odstraníme kovový vodič a aplikujeme kontrastní látku. Pro zavádění existují rovněž speciální kleště, kde středem prochází katétr. Po zavedení katétru do ductus cysticus jej pak branžemi uzavřeme. Tyto kleště tak činí celou techniku zavedení jednodušší.
Peroperační biligrafii provádíme selektivně.
2.4.3 Laparoskopická sonografie
Daleko více dnes provádíme peroperační sonografii. Laparoskopická sonografie extrahepatálních žlučových cest pomocí flexibilních sond v rukou zkušeného sonografisty má stejné procento úspěšnosti v odhalování choledocholitiázy jako peroperační biligrafie. U peroperačně zjištěné choledocholitiázy nastává volba laparoskopické explorace choledochu, konverze s choledochotomií nebo následná endoskopická sfinkterotomie a odstranění kamene z choledochu v časné pooperační době. Volba záleží na možnostech pracoviště, dostupnosti schopného endoskopisty s patřičným vybavením, eventuálně na zkušenostech operatéra.
2.4.4 Pooperační sledování
Všeobecně rizikové pacienty ukládáme na oddělení JIP. K těmto počítáme rovněž pacienty obézní. Ostatní mohou být uloženi na standardní jednotku. V den operace kontrolujeme TK, pulz, KO, sekreci z drénu, nález na břiše. Pokud pacienti nemají bolesti, analgetika neordinujeme. Antibiotika až na indikované případy nepodáváme. První pooperační den při žádné nebo malé sekreci do 20ml odstraňujeme drén. Většinou jsou pacienti již bez bolestí s obnovenou peristaltikou střevní. Při takto normálním průběhu propouštíme pacienta do ambulantní péče 2. až 3. pooperační den. Chirurgická kontrola s vytažením stehů se děje ambulantně. V případě určitého „dyskomfortu“ v dutině břišní bezprostředně v pooperačním období – přetrvávající bolesti, střevní paréza – je podezření, že se v břiše „něco děje“. Je to příznak zakrvácení do dutiny břišní, rozlití žluči nebo počínající peritonitidy. Dnes provádíme laparoskopickou cholecystektomii i v režimu jednodenní chirurgie.
2.4.5 Komplikace
Ke všem komplikacím dochází častěji v období zaškolování do laparoskopických operací. Tyto komplikace můžeme rozdělit na:
- obecné,
- specifické.
Komplikace obecné
K „obecným“ patří komplikace vzniklé nesprávně zavedenou Veressovou jehlou, a to podkožní emfyzém, emfyzém stěny břišní, pneumomediastinum a pneumotorax. Mechanismus je známý, difuze plynu přes otvory pleuroperitoneální nebo barotrauma s roztržením mediastinální pleury. Pokud se včas zjistí rozvoj pneumomediastina a pneumotoraxu, dá se stav zvládnout bez následků.Při zavádění prvního trokaru, tzv. zavádění „naslepo“, může dojít k poranění dutých a parenchymatozních orgánů v dutině břišní, u astenických pacientů pak i k poranění retroperitoneálních orgánů, nejčastěji abdominální aorty. Technika, kterou jsme si osvojili pro zavádění prvního trokaru, jak bylo popsáno již výše, minimalizuje možnost poranění orgánů dutiny břišní i orgánů retroperitonea. Dojde-li k malému poranění orgánů dutiny břišní, což zjistíme laparoskopem, můžeme toto ošetřit laparoskopicky. Pokud dojde k velkému krvácení, je nutná rychlá laparotomie s následným ošetřením podle rozsahu poranění.
Specifické komplikace
Specifické komplikace můžeme dále rozdělit na:
- komplikace malé, spíše problémy,
- komplikace závažné, velké.
Malé komplikace
Malé komplikace, spíše problémy, během laparoskopické cholecystektomie jsme schopni většinou řešit laparoskopicky.Krvácení z lůžka žlučníku běžně stavíme koagulací háčkovou elektrodou, hrotem zavřených nůžek nebo disektorem, do jehož branží zachytíme krvácející cévu. Krvácející místo si můžeme velmi dobře ozřejmit současnou trvalou irigací. Stejný postup je při použití sonografických nástrojů.Krvácení z arteria cystica. Dochází k němu velmi často při preparaci ductus cysticus. Vzhledem ke zvětšení, které laparoskopie poskytuje, vypadá toto krvácení hrozivě, hlavně tehdy, když si na laparoskopii teprve zvykáme. Toto krvácení můžeme zmírnit tlakem infundibula žlučníku proti hepatoduodenálnímu ligamentu, kdy komprimujeme arteria hepatica. V žádném případě se nesmíme snažit zastavit krvácení naslepo nakládanými svorkami. Je zde velké nebezpečí zachycení žlučovodu, eventuálně arteria hepatica do svorky. Nejlépe se osvědčil postup, kdy současně irigujeme krvácející místo a preparujeme arteria cystica. Krvácející tepnu zachytíme do branží disektoru a naložíme pak dvě svorky. Pokud nejsme schopni vyřešit krvácení laparoskopicky, je to důvod ke konverzi. Zase zde zdůrazňujeme laparoskopickou operaci oběma rukama.Perforace žlučníku. Dochází k ní u zánětlivých změn jeho stěny, která je křehká, a tahem kleští pak dojde k perforaci. Může k ní dojít i při nezměněné stěně žlučníku při preparaci z lůžka nůžkami nebo háčkem. Perforaci se snažíme uzavřít klipem nebo kleštěmi, které pak uzavírají perforaci až do dokončení izolace žlučníku. Pokud je perforace větší, zavedeme irigační sondu do lumen žlučníku, který opakovaně vypláchneme, a bez uzavření perforace dokončíme izolaci žlučníku.Volné kameny v dutině břišní souvisejí samozřejmě s perforací žlučníku. Podle literatury se ztráta kamene v břišní dutině nepovažuje za vážnou komplikaci. Přesto se snažíme volné konkrementy z dutiny břišní odstranit. Vhodným nástrojem jsou extrakční kleště, kterými můžeme větší konkrement rozdrtit na menší fragmenty a ty pak kleštěmi odstranit přes 10mm trokar. Problémem může být mnohočetná drobná litiáza, kdy se žlučník „vysype“ do podjaterní krajiny. Zde se osvědčil sáček, který zavedeme 10mm trokarem do dutiny břišní a kameny, mnohdy i se žlučníkem, vložíme do sáčku a na závěr operace exstirpujeme z dutiny břišní. Vždy velmi pečlivě vypláchneme podjaterní krajinu, zvláště jednalo-li se o empyém žlučníku.
Závažné velké komplikace
Poranění extrahepatálních žlučových cest. K této komplikaci samozřejmě dochází i u otevřené cholecystektomie. V literatuře se uvádí incidence poranění žlučových cest u otevřené cholecystektomie 0,2%. Rozvoj laparoskopické cholecystektomie, stejně jako zavedení každé nové metody, nese s sebou zpočátku i větší výskyt komplikací, včetně poranění extrahepatálních žlučových cest. V současné době je frekvence poranění žlučových cest u otevřené a laparoskopické operace srovnatelná.Může se jednat o tato poranění:
- úplné přerušení stěny žlučovodu,
- tangenciální porušení stěny žlučovodu,
- striktura žlučovodu.
Příčinou vzniku těchto komplikací je většinou technická chyba operatéra.
Při preparaci v oblasti Calotova trojúhelníku může dojít k záměně ductus cysticus za ductus choledochus (obr. 7).
Operatér se soustředí na preparaci „vývodu“, nepřesvědčí se o návaznosti infundibula žlučníku, eventuálně blízkosti horního okraje duodena. Úzké zorné pole laparoskopu, zaměřeného jen na preparovaný ductus, odvádí pozornost od okolních struktur. Rovněž přidružené krvácení znesnadňuje orientaci v této oblasti. Toto je nejčastější příčina úplného přerušení ductus choledochus. Operatér si musí pamatovat, že v krajině Calotova trojúhelníku se velmi často vyskytují anomálie jak žlučových vývodů, tak průběhu cév. Pokud operatér zaklipuje a přeruší ductus choledochus a pokračuje dále v preparaci domnělého ductus cysticus, klipuje pak ductus hepaticus v domnění, že se jedná o aberantní žlučovod. Tím dojde k vytětí ductus hepatocholedochus a resekovaná část pak zůstává součástí preparátu.
Tangenciální poranění
K tangenciálnímu poranění dochází nejčastěji při nešetrné izolaci ductus cysticus háčkem nebo nůžkami nebo při nakládání klipů na ductus cysticus.
Striktura žlučovodu
Striktura pak může vzniknout časně při nekontrolovaném naložení klipů, nejčastěji při stavění krvácení v oblasti Calotova trojúhelníku. K pozdní stenóze pak může dojít na podkladě termického poškození společného žlučovodu s následnou strikturou. Jde o následek neúměrného používání koagulace v blízkosti choledochu.
Jestliže během laparoskopické cholecystektomie máme pochybnosti, zda jsme nepřerušili ductus choledochus, provedeme peroperační biligrafii. Kanylu zavádíme místem poranění. Když biligrafie prokáže protětí, tzn. že se plní jen distální úsek ductus choledochus a nenaplní se intrahepatální žlučovody, jsme nuceni operaci konvertovat a řešit poranění.Pokud v pooperačním období přetrvávají bolesti, objevuje se ikterus, drén odvádí žluč nebo se potvrdí sonograficky kolekce žluče v podjaterní krajině nebo se vyvine biliární peritonitida, je pravděpodobné, že došlo k poranění extrahepatálního žlučovodu.
Pro potvrzení nebo vyloučení této diagnózy má největší přínos vyšetření ERCP. Úplné stop kontrastu znamená přerušení a zaklipování ductus choledochus, únik kontrastu při naplnění intrahepatálních žlučových cest pak znamená nástěnné poranění, eventuálně únik z pahýlu ductus cysticus. Vzhledem k závažnosti této problematiky je zcela na místě zmínit se, jak ošetřit peroperační poranění žlučových vývodů. Pro osud nemocného je důležité, aby bylo poranění rozpoznáno a dobře ošetřeno hned při operaci. Podmínky pro reparaci jsou nejlepší, dají se dobře rozpoznat přerušené konce duktu, tkáně se dají dobře mobilizovat.
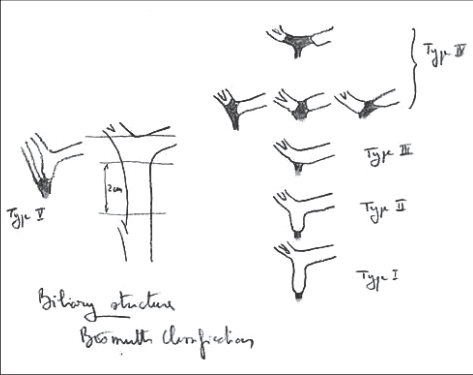
Obr. 8 – Bismuthova originální klasifikace a kresba (I. až V. typ) poranění extrahepatálních žlučových cest
Pokud ERCP vyšetření v pooperační době prokáže jen malé nástěnné poranění, může být toto ošetřeno zavedením stentu. Stejně můžeme ošetřit únik kontrastu při uvolnění klipů z ductus cysticus. Při větším nástěnném poranění je nutná reoperace s následnou suturou, již zajistíme T-drénem, který je zaveden mimo tuto suturu. Úplně přerušený ductus choledochus lze rovněž ošetřit suturou na T-drénu. V případě, že je ductus choledochus přerušen se ztrátou své délky, je lépe napojit centrální pahýl na exkludovanou kličku jejuna podle Rouxe.
Z hlediska léčebné taktiky je důležité rozdělení poranění žlučových cest podle lokalizace. Originální, nejčastěji užívanou klasifikací navrhl Bismuth (obr. 8).
- Poranění v oblasti papily Vaterské a retroduodenálního průběhu choledochu. K těmto poraněním dochází při sfinkteropapilotomii a dále při resekcích žaludku. Při preparaci duodena během resekce dochází k prošití nebo přerušení žlučových cest. Tato poranění, nejsou-li včas rozpoznána a léčena, vedou k rozvoji pankreatitidy a retroperitoneální flegmony se špatnou prognózou. Bližší poučení je třeba hledat v literatuře o komplikacích sfinkteropapilotomie a resekcí žaludku. Zvláštním typem poranění je tzv. desinserce papily. Při izolaci zadní stěny duodena od pankreatu dojde k přerušení žlučových cest těsně při vstupu do stěny dvanácterníku. Ošetření spočívá v reinzerci žlučovodu do duodena či Rouxovy kličky.
- K poranění hepatocholedochu dochází nejčastěji při cholecystektomii. Při dostatečném průsvitu žlučovodu a dobré kvalitě stěny je možné provést suturu poranění nebo i kompletní end-to-end anastomózu na T-drénu. Ten je třeba vždy zavést mimo vlastní suturu (obr. 9). Tento způsob je nevhodný při větším defektu stěny, kdy by byla sutura pod napětím, nebo při žlučových cestách velmi malého průsvitu. Pak je lépe našít anastomózu v hilu, jak je uvedeno dále. Velmi často se setkáváme s tím, že chirurg poranil žlučové cesty výše, než předpokládal. Anatomické poměry je nutné si pečlivě ověřit sondáží a cholangiografií.
- Nejzávažnější je poranění v jaterním hilu, tj. v oblasti junkce obou hepatiků. Zde je nejvhodnější založit hepatikojejunální anastomózu Rouxovou kličkou.Vedle lokalizace je pro léčebnou techniku důležitý i rozsah poranění. Bodová poranění se po sutuře hojí mnohem lépe než protětí větší části cirkumference žlučovodu. K sekundárnímu jizvení dochází po sutuře poškozené stěny (např. elektrokoagulací), nebo byla-li sutura pod napětím po ztrátovém poranění.Po laparoskopické cholecystektomii jsou častější termická poranění, která se projeví únikem žluči až v pooperačním období. Častější je i sklouznutí svorky z pahýlu ductus cysticus. Naložením svorky na hepatocholedochus může dojít k jeho zúžení.Bohužel, jen menší část poranění žlučových cest je diagnostikována během operace. Častěji jsou cholaskos či známky obstrukce žlučových cest rozpoznány až v pooperačním obodbí. Rozhodující význam pro stanovení diagnózy má ERCP.
Technika hilové spojky a drenáže
Abychom dosáhli co nejširšího průsvitu hepatojejunální anastomózy, prodlužujeme ji směrem na levý ductus hepaticus a zakládáme tzv. Couinaud-Heppovu anastomózu (obr. 10).Předpokladem úspěchu je dodržení zásady mukomukózní spojky s přesnou adaptací sliznice žlučovodu na sliznici jejuna. V nepřehledném terénu může usnadnit adaptaci sliznice šití spojky na zavedeném drénu. Spojku šijeme v jedné vrstvě vstřebatelným stehem. Není jednotný názor na to, zda má být spojka po operaci drénována. Dostatečně širokou spojku s dobrou adaptací sliznice na sliznici není třeba drénovat, protože drenáž je vždy pro nemocného nepříjemná. Spojku je lépe drénovat u obtížněji zakládaných anastomóz, kde často nelze dosáhnout exaktní mukomukózní adaptace, a při úzkých žlučových cestách. Drén zde má funkci protézy, na které se anastomóza hojí. Boční otvory v drénu zajišťují u ne zcela těsnící spojky odtok žluči z jater do střeva.Absolutní nutností je drenáž tam, kde je junkce hepatiků zničená. Vytváříme hluboko v hilu, v jaterním parenchymu, tzv. bezstehovou anastomózu. Přímý mukomukózní steh zde založit nelze (obr. 11a, b, c, d).Ideální je ošetřit poranění ihned po jeho vzniku a rozpoznání. Ošetření by mělo být definitivní, protože každá další reoperace zhoršuje naději na dobrý výsledek rekonstrukce. Jedná se o výkon vysoce delikátní a zodpovědný, který by měl provádět chirurg s dostatečnými zkušenostmi. Tyto požadavky jsou někdy obtížně splnitelné. Zvláště vyžaduje-li ošetření bezprostředně rozpoznané v průběhu cholecystektomie založení hilové anastomózy, nemusí mít každý operující dostatečné předpoklady k dokončení této operace. Podle okolnosti je třeba vždy zajistit nejkvalifikovanější způsob ošetření.Tam, kde je poranění rozpoznáno až v pooperačním období, a u opakovaných reoperací je absolutně nutné, aby operaci prováděl chirurg s dostatečnými zkušenostmi s reoperacemi na žlučových cestách. Iatrogenní poranění je lépe koncentrovat do specializovaných center. Odsunutí operace o několik dní nezhoršuje obvykle vyhlídky na optimální výsledek. Nesrovnatelně větším rizikem pro nemocného je neadekvátní ošetření poranění, které si vyžádá v budoucnu reoperaci.
Poranění střeva
K tomuto poranění může dojít jednak při zavádění trokarů, jak již bylo zmíněno, dále při preparaci v zánětlivém infiltrátu, do kterého může být zavzato např. duodenum. Pokud je poranění zjištěno během laparoskopické cholecystektomie, je na chirurgovi, zda poranění ošetří laparoskopicky stehem, nebo je důvodem ke konverzi. V pooperačním období může být peritonitida zapříčiněna právě poraněním střeva.Krvácení, které operatér není schopen zvládnout laparoskopicky, je rovněž důvodem ke konverzi. Jedná se většinou o krvácení z arteria cystica, krvácení z lůžka u zánětlivě změněných žlučníků. Příčinou hemoperitonea v pooperační době je často uvolněný klip na arteria cystica. Jde-li o krvácení z lůžka žlučníku, pak při reoperaci již zdroj mnohdy nenajdeme.
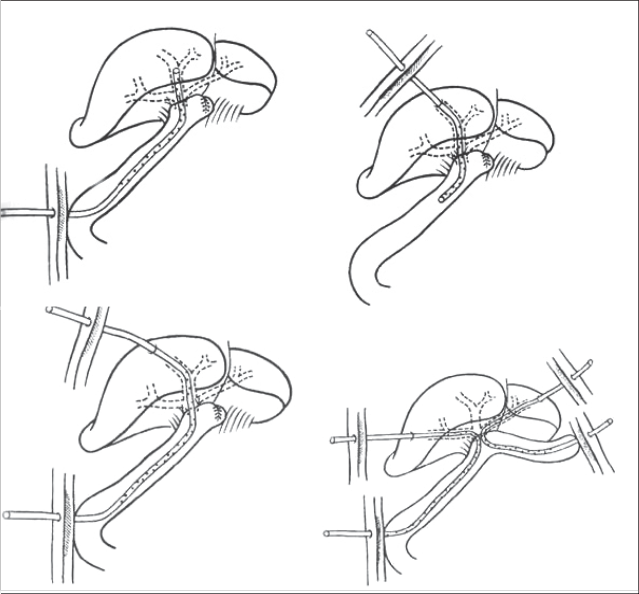
Obr. 11 – Různé typy hepatikojejunální drenáže
a) drenáž podle Voelckerova principu
b) transhepatická (diahepatická) drenáž
c) diahepatická drenáž bez konce „U“
d) dvojitá diahepatická drenáž
Biliární peritonitida je způsobena nejčastěji prosakováním žluče z lůžka žlučníku, další příčinou je aberantní žlučovod a nakonec léze žlučovodu. Pokud při laparoskopické cholecystektomii přerušíme aberantní žlučovod, je lépe jej uzavřít klipem než koagulací. Po koagulaci dochází časem k uvolnění koagulační nekrózy a opětovnému výronu žluče. Pokud drén dostatečně odvádí, není nutná revize, aberantní žlučovod se časem uzavře spontánně. Ošetření biliární peritonitidy při lézi žlučových vývodů bylo již uvedeno výše.Hnisavé komplikace. Příčinou hnisavých komplikací v dutině břišní, tj. abscesu a difuzní peritonitidy, může být poranění střeva, empyém žlučníku nebo rozsáhlý hematom v subhepatálním prostoru. Při klinických příznacích svědčících pro tuto komplikaci provádíme vyšetření sonografické, ev. vyšetření CT. Pokud se jedná o absces, je diagnostika pomocí těchto vyšetření jasná, horší je to už u difuzní peritonitidy. Stejně jako u biliární peritonitidy nám toto vyšetření mnohdy nic neozřejmí, spoléháme se pak jen na klinické vyšetření. Ošetření abscesu v subhepatální oblasti může být provedeno cílenou drenáží pod sonografickou nebo CT kontrolou. Velké abscesy a difuzní peritonitida vyžadují laparotomii, laváž dutiny břišní, čili ošetření jako peritonitidy z jiné příčiny.
2.5 Laparoskopická cholecystektomie u akutní cholecystitidy
Indikace a příprava
Před nástupem éry laparoskopických cholecystektomií spočívalo chirurgické léčení akutní cholecystitidy v časné otevřené cholecystektomii.Tento postup se vyvinul na základě studií, které začaly zavrhovat původní terapeutické schéma: zklidnění akutní cholecystitidy, propuštění pacienta a následné přijetí k plánované operaci, nejčastěji několik týdnů po první dimisi. Současnou tendenci operovat pokud možno co nejdříve po přijetí pacienta s akutní cholecystitidou zastává dnes převážná část chirurgů.Ještě nedávno byly akutní cholecystitida a empyém žlučníku považovány za relativní kontraindikace laparoskopické cholecystektomie. Rovněž práce z řady dalších center referovaly o vysokém podílu konverzí, když se lékaři pokoušeli operovat těžce zanícený žlučník, a proto tvrdili, že takový stav je nutno považovat za kontraindikaci laparoskopického výkonu. Většina konverzí byla elektivních a hlavním faktorem byly zánětlivé změny stěny žlučníku, ať už se srůsty, nebo bez nich. Dnes není akutní cholecystitida kontraindikací k laparoskopické cholecystektomii.
Technika a taktika operace se neliší v zásadě od elektivní cholecystektomie.
Komplikace a jejich řešení
Laparoskopická cholecystektomie u akutní cholecystitidy je bezpečná a je spojená s prokazatelně kratší pooperační hospitalizací ve srovnání s klasickou cholecystektomií. Je jen věcí operatéra, aby v obtížném terénu Calotova trojúhelníku včas zvolil nevynucenou konverzi, která, je-li provedena včas, zabrání nejčastějším možným komplikacím, vyplývajícím z nepřehledných srůstů v dané oblasti: poranění žlučovodů, nekontrolovanému krvácení z a. cystica nebo a. hepatica, poranění stěny duodena či tračníku. Pokud jsou tyto komplikace řešeny během jedné operace, nemusí být následky závažné. Při peroperačně nepoznaných poraněních stoupá exponenciálně procento neúspěchů.
2.6 Laparoskopické výkony na žlučových cestách
Od roku 1987, kdy provedl Mouret (Francie) první laparoskopickou cholecystektomii, se tato metoda postupně stala metodou volby léčení cholecystolitiázy. Aby tento výkon splňoval v naprosté většině požadavky miniinvazivní chirurgie – pooperační komfort s krátkou rekonvalescencí a hospitalizací, s časným návratem do pracovního procesu a dobrým kosmetickým efektem, je nutno umět šetrně vyřešit i choledocholitiázu, která se vyskytuje u 5–15% nemocných s cholecystolitiázou. Současné možnosti terapie choledocholitiázy jsou:
- endoskopické odstranění kamenů ze žlučovodu, a to před či po laparoskopické cholecystektomii,
- perkutánní odstranění kamenů transhepaticky či kanálkem po T-drénu,
- laparoskopické vyjmutí kamenů,
- klasická chirurgická revize žlučových cest s odstraněním konkrementů z hepatocholedochu.
Volba nejvhodnější metody závisí nejen na stavu konkrétního nemocného, ale i na zkušenostech a zvyklostech pracoviště. I přesto, že se snažíme snížit nutnost otevřené chirurgické choledocholitotomie na minimum, někdy se jí nevyhneme.
Indikace
Většinou lze dnes cholelitiázu vyřešit pomoci ERCP. Laparoskopickou revizi žlučových cest indikujeme v případě neúspěchu endoskopické extrakce konkrementů z choledochu nebo v případě náhodného nálezu širokých žlučových cest peroperačně (nedostatečně vyšetřených před operací). Kontraindikace k laparoskopické revizi žlučových cest je u těch pacientů, kde je laparoskopie obecně kontraindikována (respirační, oběhová insuficience atd.). Z chirurgického hlediska prakticky nemá laparoskopická revize žlučových cest kontraindikace. Laparoskopicky totiž můžeme v dnešní době provést všechny výkony jako při klasické revizi žlučových cest (peroperační cholangiografie a endosonografie, peroperační choledochotomie, peroperační choledochoskopie). Zkušenost s laparoskopickými operacemi je nejdůležitějším momentem při rozhodování chirurga, zda revidovat žlučové cesty klasicky či laparoskopicky.
Operační technika
K laparoskopické revizi žlučových cest přistupujeme většinou po peroperační cholangiografii nebo peroperační endosonografii. Cholangiografii provádíme vpichem speciální jehly přes stěnu břišní a zavedením katétru jehlou do ductus cysticus (obr. 12a,b).Endosonograf zavádíme do dutiny břišní některým z již zavedených trokarů. Endosonografie se zdá být citlivější metodou v diagnostice litiázy žlučových cest.Stiegmann u pacientů s choledocholitiázou zdůraznil senzitivitu endosonografie u 89% a peroperační cholangiografie u 53% pacientů. Bohužel zatím není endosonografie na všech pracovištích dostupná. Při nálezu drobné choledocholitiázy se snažíme konkrementy transcysticky extrahovat nebo protlačit do duodena po eventuální papilotomii. Postup vypadá tak, že incizí na ductus cysticus po předchozí cholangiografii zavádíme do choledochu Dormia kličku a snažíme se extrahovat konkrementy transcysticky (obr. 13).
Neuspějeme-li, pokusíme se stejnou transcystickou cestou protlačit konkrementy do duodena. V případě neúspěchu můžeme provést papilotomii. Pak je protlačení konkrementů do duodena daleko jednodušší. Neúspěch nebo velikost konkrementů nás nutí k choledochotomii laparoskopicky. Délku choledochotomie volíme podle velikost konkrementů (převážně 1,5–2 cm). Následuje extrakce konkrementů Dormia kličkou nebo za kontroly choledochoskopem. Velké konkrementy je možno drtit litotryptory různého druhu. Před uzávěrem choledochotomie důkladně cholangioskopicky revidujeme žlučové cesty. Ductus choledochus uzavíráme v jedné vrstvě – pokračujícím nebo jednotlivými stehy. Drenáž žlučových cest je otázkou zvyklosti jednotlivých pracovišť. Můžeme ji provést transcysticky nebo klasicky T-drénem (obr. 14).Není-li přetlak ve žlučových cestách, provádíme suturu choledochotomie bez drenáže. Tento algoritmus laparoskopické revize žlučových cest se ničím neliší od algoritmu klasické revize. Rozhodujícím faktorem je zase zkušenost chirurga u laparoskopických operací.Nejčastější komplikací při laparoskopické revizi žlučových cest jsou reziduální konkrementy a insuficience choledochotomie s únikem žluče do dutiny břišní. Jako prevenci reziduální choledocholitiázy provádíme vždy před ukončením zákroku podle možností kontrolní cholangiografii nebo cholangioskopii nebo endosonografické vyšetření žlučových cest. V případě pozitivního nálezu záleží na chirurgovi, zda se rozhodne k opakované laparoskopické revizi, endoskopické revizi či revizi klasické. Postup je určitě závislý od zkušeností chirurga a zvyklostí pracoviště. Další komplikací je insuficience choledochotomie, kterou můžeme zase podle zkušeností chirurga a zvyklostí pracoviště ošetřit endoskopicky (stenty), laparoskopicky (resutura, T-drén, drenáž okolí) nebo klasicky (stejný postup). Méně častými komplikacemi při laparoskopické revizi žlučových cest jsou poranění okolních orgánů (játra, žaludek, duodenum, bránice).
Výsledky
Choledocholitiáza se vyskytuje u 5–15% nemocných s cholecystolitiázou. V 90% se podaří extrahovat konkrementy endoskopicky. Ve zbývajících 10% jsme nuceni revidovat žlučové cesty laparoskopicky nebo klasicky. Nejdůležitějším faktorem je při rozhodování zkušenost chirurga-laparoskopisty a zvyklost pracoviště. V každém případě musí být laparoskopická revize žlučových cest prováděna na pracovištích s výborným technickým vybavením (endosonograf, cholangioskop atd.) a hlavně odborně fundovaným a zkušeným personálem. Při řešení choledocholitiázy je důležitá časná diagnostika, nejlépe předoperační, a dále pak spolupráce endoskopisty se zkušeným chirurgem-laparoskopistou.
2.7 Konverze a klasická cholecystektomie
I v dnešní době, kdy se provádí více než 95% cholecystektomií laparoskopicky, musí zkušený chirurg ovládat klasický přístup – klasickou cholecystektomii a klasickou revizi žlučových cest.Uvedeme proto základní klasické výkony, které by měl provádět zkušený chirurg na daném pracovišti, nebo by měl být pacient transportován do centra, které má s těmito komplikacemi zkušenosti – vždy se totiž jedná o pacienta, vždy se totiž může jednat o jeho život.Proto zmíníme zásady otevřených klasických výkonů, které platí pořád.
- Anterográdní cholecystektomie, při které odstraňujeme žlučník od fundu subperitoneálně tak, že nařízneme u jater serózu fundu žlučníku a ten postupně vyloupneme z jaterního lůžka, takže zůstane viset na cystické arterii a cystiku, které se po odstřižení žlučníku podvážou. Nebezpečí této metody, zejména při mnohočetné cholecystolitiáze, je v možnosti zatlačení konkrementů průchodným cystikem do choledochu.
- Retrográdní cholecystektomie spočívá v přístupu opačném: nalezení, vypreparování a podvaz arteria cystika a ductus cystikus, po jejich přerušení se žlučník odstraňuje směrem od krčku k fundu. Tento způsob zajišťuje přehlednost operačního pole a ozřejmění struktur v ligamentu hepatoduodenálním před samotnou cholecystektomií. Použití jednoho nebo druhého způsobu záleží především na zvyklostech a zkušenostech toho kterého pracoviště a operační situace u daného pacienta.
Nebezpečí cholecystektomie může být v poranění společného hepatiku, junkce hepatiků, choledochu, především však arteria hepatica propria a její pravé větve, někdy i vena portae. Tato poranění mohou být podmíněna i častými anomáliemi v průběhu těchto struktur, ztíženým přehledem při přemístění anatomických útvarů pozánětlivými srůsty nebo jindy operováním bez získání nutného přehledu v operačním poli.
Obecně platí: nemáme-li jistotu bezpečného laparoskopického výkonu, konvertujeme a řešíme situaci ku prospěchu pacienta.
- Cholecystoanastomózy biliodigestivní jsou paliativní výkony, jimiž obcházíme překážku ve žlučových cestách a dosahujeme odtoku žluče do zažívacího traktu a vymizení ikteru. Žlučník lze spojit se žaludkem (cholecystogastroanastomóza), s duodenem (cholecystoduodenoanastomóza) (obr. 15) nebo s jejunem (cholecystojejunoanastomóza) (obr. 16). Při všech těchto výkonech ukládáme do podjaterní krajiny drén, který slouží k odvádění žluče nebo krve. Drén odstraňujeme za 48 hodin, jestliže z něj není vylučována patologická sekrece. Před těmito anastomózami mají dnes jednoznačně přednost endoskopické výkony: stenty a drenáže žlučových cest.
Choledochotomie: otevření žlučovodu, doplněné exploraci žlučových cest.Indikace k revizi choledochu:
- prokazatelné konkrementy, které nemůžeme endoani laparoskopicky extrahovat,
- obstrukční ikterus a cholangoitida neřešitelné endoči laparoskopicky,
- cholangiograficky předoperačně a peroperačně prokázané konkrementy v choledochu nelze endo-ani laparoskopicky extrahovat,
- dilatace hepatocholedochu a stenózy papily neřešitelné endoskopicky.
Choledochotomii pak děláme v supraduodenálním úseku choledochu většinou podélně v dlouhé osežlučovodu. Instrumentálně pomocí Bakešovy sondy se pak vyšetří jak intrahepatické, tak extrahepatické žlučové cesty. Konkrementy se odstraňují kleštěmi, lžičkami, Fogartyho katétrem či Dormiovou kličkou a také výplachy.Výkon musí být vždy ukončen zjištěním průchodnosti papily její sondáží. Ještě peroperačně lze provést cholangiografickou kontrolu pomocí balonkem zaklíněné cévky, a to směrem proximálním a distálním, nebo prohlédnout žlučovody pomocí choledochoskopu, který navíc dovoluje cílený odběr materiálu k bioptickému vyšetření (např. z papily). Choledochotomie se pak uzavírá vodotěsně atraumatickými stehy buď primárně celá, nebo se pak do choledochu vkládá dočasná drenáž (nejčastěji se užívá Kehrův T-drén) (obr. 17), která slouží:
- k dekompresi žlučových cest v pooperačním období, kdy se následkem instrumentálního vyšetření papily předpokládá její edém a spazmus sfinkteru a stoupá tlak ve žlučovodech,
- ke kontrolní cholangiografii, a to hned po uzavření choledochu (sekundární peroperační cholangiografie) a dále v sedmém až desátém dni po operaci jako pooperační cholangiografie,
- k instrumentálnímu odstranění možných ponechaných kamenů,
- k dekompresi u cholangoitid, pankreatitid nebo při podezření na ponechanou překážku.Jakmile se obnoví po operaci normální funkce zažívacího traktu, začneme T-drén postupně zavírat (asi od 5. pooperačního dne) a po cholangiografické kontrole jej odstraníme (kolem 10. dne). Žlučová píštěl, která po jeho odstranění zbude, se uzavře spontánně, jestliže je volný odtok žluče do duodena.Papilosfinkterotomie je výkon na papile a Oddiho svěrači (obr. 18). Při papilotomii jde o protětí papilární části a při papilosfinkterotomii ještě navíc o protětí (většinou částečné) Oddiho svěrače. Dnes se tyto výkony provádějí výlučně endoskopicky, výjimečně chirurgicky.
Indikace: kaménky zaklíněné v terminální části žlučovodu, které nelze odstranit shora z choledochotomie, vypadnou po sfinkterotomii zpravidla rychle do duodena.
Anastomózy hepatocholedochu s některou částí zažívacího traktu (žaludkem, duodenem, jejunem) jsou indikovány (obr. 19a,b, 20a,b):
- u kongenitálních atrézií operabilního typu a u cystických dilatací hepatocholedochu,
- u striktur distálních částí choledochu po jeho poranění a zánětech,
- u chronických pankreatitid se stenózou pankreatické části choledochu a s dilatací jeho proximálního úseku,
- u mnohočetných konkrementů v nitrojaterních vývodech, které nelze peroperačně odstranit,
- u inoperabilních nádorů hlavy pankreatu, papily nebo terminálního choledochu, které působí obstrukci žlučovodu.
Provedení: nejvýhodnější, z hlediska prevence vzestupné cholangoitidy, je choledochojejunoanastomóza nebo hepatikojejunoanastomóza s vyřazenou (z pasáže) jejunální kličkou podle Rouxe – tzv. Y anastomóza, kterou užíváme jako definitivní řešení při defektu žlučovodu podmíněném benigní příčinou, tedy po jeho poranění, vytětí, dlouhodobých zánětlivých strikturách apod. (obr. 19b).V ostatních případech se nejčastěji užívá choledochoduodenoanastomóza (obr. 20) a jen výjimečně choledochogastroanastomóza, obě založené laterolaterálně.
Anastomózy hilové jsou indikovány primárně při vrozených stenózách a atréziích hepatiku, při jeho operačním poranění nebo po resekci nádoru společného hepatiku nebo cystiku a nejčastěji při reoperacích pro striktury a zevní píštěle hepatiku zaviněné předchozím výkonem nebo také při obstrukci dříve založené biliodigestivní anastomózy s hepatikem.
Jde většinou o anastomózu s kličkou jejuna, do které se vústí soutok obou hepatiků (obr. 19), případně každý hepatikus zvlášť, jestliže je poškození vysoko. Tyto anastomózy se zakládají většinou na modelujícím drénu, který se odstraní po několika měsících. Bylo o nich již také pojednáno v souvislostí s ošetřením poranění žlučových cest (obr. 10).
Anastomózy intrahepatální se zakládají u vrozených atrézií intrahepatálních jako nejistý pokus o záchranu dítěte nebo u jiných stenóz vysoko v jaterním hilu, které jsou nedostupné k založení anastomóz dříve uvedených. Ve většině případů se našívá exkludovaná Rouxova klička (obr. 21).
Další indikací jsou zhoubné nádory s obstrukční žloutenkou, lokalizované v hepatocholedochu nebo ve spojení hepatiků, jestliže v játrech není rozsev metastáz. Jde tu o spojení intraparechymatózně uložených jaterních vývodů s kličkou jejuna. Jelikož sevětšinou jedná o velmi nepříznivou prognózu, dáváme přednost šetrné endoskopické stentáži (8).
2.8 Laparoskopická cholecystektomie v režimu jednodenní chirurgie
První zprávu o laparoskopicky provedené cholecystektomii v režimu jednodenní chirurgie publikovali v roce 1990 E. J. Reddick a D. O. Olsen.Zařazení laparoskopické cholecystektomie do režimu jednodenní chirurgie není zatím na mnohých chirurgických pracovištích běžně akceptováno. Umožnění této léčby nemocným se symptomatickou cholecystolitiázou je vhodné na pracovištích s velmi nízkým výskytem komplikací. Pacienti mohou být spolehlivě a bezpečně propuštěni v den operačního výkonu, eventuálně do 24 hodin po jeho ukončení.
Klinický soubor
Obr. 21 – Anastomóza hilová
a) rozšíření žlučovodu nástřihem levého hepatiku,
b) po založení anastomózy s kličkou jejuna
V Centru miniinvazivní chirurgie Nemocnice Podlesí v Třinci byla první laparoskopická cholecystektomie provedena 3. prosince 1991. Po nutné stavební úpravě nemocnice a operačních sálů bylo vybudováno Centrum jednodenní chirurgie, kde nedochází ke křížení ambulantní a nemocniční části zdravotnického zařízení. Následně od začátku roku 2003 byla zahájena i léčba pacientů s cholelitiázou v rámci programu jednodenní chirurgie.K jednodenní chirurgické léčbě jsou indikováni přísně selektovaní pacienti splňující anesteziologická, chirurgická a sociální kritéria a samozřejmě souhlasící s tímto léčebným postupem.Pacienti indikovaní k jednodenní cholecystektomii byli vždy zařazeni na úvod operačního programu. Operační skupinu tvoří chirurg s asistentem, instrumentující sestra a anesteziolog s anesteziologickou sestrou.
Na tomto pracovišti byly operace prováděny ve „francouzské pozici“. Operatér stojí mezi nohama pacienta. Subhepatální drenáž je zakládána většinou pro krátkodobou kontrolu důkladnosti vykonané hemostázy při nutnosti koagulace v lůžku po cholecystektomii. Antibiotická profylaxe byla indikována individuálně. Pooperačně byl pacient uložen ke sledování na lůžko Centra jednodenní chirurgie. Do domácí péče byl propuštěn po kontrole anesteziologem a chirurgem a po pohovoru s ním a s jeho doprovázející osobou. Současně byla informována agentura domácí péče.
První pooperační den ráno pacienta navštívila zdravotní sestra spolupracující agentury domácí péče, která následně informovala lékaře Centra jednodenní chirurgie o stavu operovaného. Kontrola v našem zdravotnickém zařízení se většinou uskutečnila 7. a 21. pooperační den.
První laparoskopická cholecystektomie byla v programu jednodenní chirurgie provedena na našem pracovišti 27. února 2003. Od 27. února 2003 do 30. června 2006 jsme tento operační postup v léčbě cholecystolitiázy plánovali u 93 pacientů, tj. u 15,4%ze všech 618 nemocných indikovaných v tomto období k plánované či urgentní laparoskopické cholecystektomii. V prezentovaném souboru operovaných bylo 72 žen a 21 mužů. V den operace odešlo do domácího ošetření 84 pacientů, u 9 operovaných bylo nutné setrvání na lůžku zdravotnického zařízení první pooperační noc. Tito pacienti byli propuštěni do domácí péče první pooperační den ráno, všichni do 24 hodin od ukončení operačního výkonu.
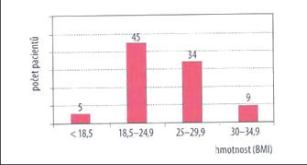
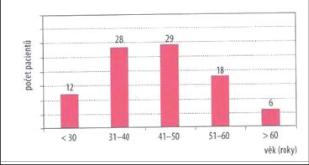
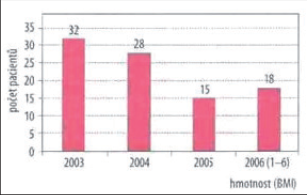
V prezentovaném souboru dominovali pacienti mezi čtyřiceti a padesáti lety, kteří tvořili dohromady 61,3% operovaných. Bližší rozdělení souboru pacientů podle věku ukazuje graf 1.K jednodenní laparoskopické cholecystektomii jsou indikováni zejména pacienti s nižším operačním rizikem zařazení do kategorie ASA I a II. V našem souboru bylo operováno 14 pacientů klasifikace ASA I (15,0%), 65 pacientů ASA II (69,9%), 13 pacientů ASA III (14,0%) a 1 pacient s ASA IV (1,1%). Operovaný pacient s ASA IV byl však po operaci po zhodnocení stavu ponechán první pooperační noc v našem zdravotnickém zařízení.Normální tělesnou hmotnost mělo 48,4% operovaných, nadváhu mělo 36,6% a obézních bylo 9,7% pacientů. Rozdělení souboru pacientů podle tělesné hmotnosti znázorňuje graf 2.
Výsledky
Z 93 pacientů, u kterých jsme provedli laparoskopickou cholecystektomii v programu jednodenní chirurgie, odešlo do domácího ošetření 84 pacientů (90,3%) v den operačního výkonu. U 9 operovaných (9,7%) jsme se rozhodli pro prodloužení pobytu na lůžku Centra jednodenní chirurgie o první pooperační noc. Důvodem k tomuto rozhodnutí byla u pěti pacientů vyšší serosanguinolentní produkce do subhepatálně lokalizovaného drénu. Dva operovaní měli pooperačně výraznější bolestivou reakci. U jednoho pacienta jsme se rozhodli k tomuto postupu vzhledem k závažné komorbiditě (ASA IV). Jeden operovaný zůstal ve zdravotnickém zařízení na vlastní žádost ze strachu před možnými komplikacemi. Všech devět pacientů však bylo propuštěno do domácí péče první pooperační den, tzn. do 24 hodin od ukončení operačního výkonu. Ani u jednoho operovaného jsme nezaznamenali peroperační komplikaci a taktéž žádný z pacientů nemusel být rehospitalizován (graf 3).V histopatologickém nálezu byly ve 45 preparátech přítomny známky chronické cholecystitidy, ve 45 případech nebyl popsán chronický ani akutní zánět a ve třech preparátech byl přítomen nález akutního flegmonózního zánětu.Výhoda pro pacienty s cholelitiázou operované v programu jednodenní chirurgie spočívá ve výraznějším pohodlí. U takovéhoto typu operace je však nutné precizní plánování ve snaze vyhnout se vzniku komplikací. Zkušenosti publikované různými autory a srovnané s autory našimi jsou shrnuty v tabulce 1.Potenciálními bariérami pro uskutečnění jednodenního programu jsou medicínské, subjektivní a institucionální překážky. Medicínskými bariérami jsou zejména komorbidita pacienta, pooperačníbolest a zvracení v pooperačním období, které jsou překážkami propuštění nemocného v den operačního výkonu. Překážkou při indikaci k této léčbě v jednodenním režimu může být rovněž špatná multidisciplinární komunikace a nedostatečná spolupráce ze strany pacienta při plánování.
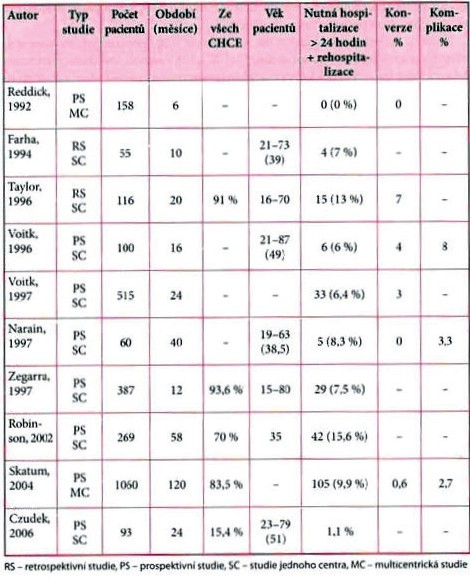
Tab. 1 – Publikované sestavy
laparoskopických cholecystektomií
v jednodenním režimu
(podle Czudek 2009)
Oponenti ambulantní laparoskopické cholecystektomie argumentují možným rizikem časných vážných pooperačních komplikací, jakými jsou např. krvácení z arteria cystica nebo z lůžka po odstranění žlučníku. Právě při obavě z možného rizika je však vhodné ponechat pacienta první pooperační noc ke sledování na lůžku zdravotnického zařízení a propustit ho až po 24 hodinách od ukončení operačního výkonu po vyloučení možné komplikace. U takto sledovaných pacientů není statisticky významný rozdíl ve vzniku komplikací v porovnání se skupinou pacientů hospitalizovaných pooperačně tři až čtyři dny.
Campanelli a kol. ve své práci předkládají návrh na selekci skupiny pacientů indikovaných k laparoskopické cholecystektomii s možným zařazením do programu jednodenní chirurgie. Kritériem pro zařazení pacienta do takového programu má být věk pod 70 let, ASA I a II, index tělesné hmotnosti (BMI) menší než 35, nepřítomný anamnestický údaj o obstrukčním ikteru, nepravděpodobná přítomnost choledocholitiázy a samozřejmě souhlas pacienta s takto vedenou léčbou. Jako kritérium pro vyřazení z programu jednodenní chirurgie udávají věk nad 70 let, ASA III a IV, index tělesné hmotnosti (BMI) větší než 35, akutní cholecystitidu, pozitivní anamnézu obstrukčního ikteru a strach pacienta z takto provedené operace. Nevhodný k zařazení je i pacient žijící o samotě, pacient, který bydlí ve velké vzdálenosti od nemocnice či nemá k dispozici telefon.Podle Voylesa a kol. jsou nejčastějšími příčinami nezařazení pacienta do režimu ambulantní operace akutní cholecystitida, věk nad 65 let, plánovaný sdružený operační výkon, vysoké riziko možné choledocholitiázy, přidružené onemocnění operovaného, obezita a gravidita. Ale i u pacientů s vyšším operačním rizikem daným věkem pacienta a přidruženými onemocněními je laparoskopická cholecystektomie v režimu ambulantní chirurgie chápána jako metoda možná a bezpečná. Tato skupina pacientů je však zatížena signifikantně vyšším rizikem nutné změny pooperační strategie ve smyslu ponechání pacienta v nemocniční péči.
Voitk ve své práci uvádí nutnost takovéto změny až u 28% operovaných vysoce rizikových pacientů. V našem souboru byl do režimu ambulantní cholecystektomie zařazen jeden pacient s ASA IV, který však byl po operaci na základě zhodnocení stavu ponechán první pooperační noc ve zdravotnickém zařízení. U tohoto operovaného už samotná indikace k ambulantní cholecystektomii byla problematická.Průměrná doba nutného sledování operovaných na pooperačním pokoji je udávána od 180 minut do 7,5 hodiny. Fiorello a kol. udávají jako prediktivní faktor úspěšného časného propuštění pacienta trvání operačního výkonu. U skupiny ambulantně operovaných pacientů trval operační výkon průměrně 62 minut oproti 82 minutám ve skupině pacientů ponechaných na lůžku pooperačního pokoje po dobu celé noci. Přibližně 20% laparoskopicky operovaných pacientů v režimu jednodenní chirurgie preferuje setrvání na lůžku zdravotnického zařízení po dobu první noci po operaci. Robinson a kol. udávají možnost ambulantní laparoskopické cholecystektomie u 70% z neselektovaného souboru pacientů operovaných v Denver Health Medical Center.
Skattum a kol. v prospektivní studii prezentují soubor 1060 pacientů operovaných v období 10 let v režimu jednodenní chirurgie. U 9,9% operovaných byla nutná hospitalizace a u 6,6% po primárním propuštění pak rehospitalizace. Nejčastější příčinou přijetí pacienta k rehospitalizaci byly všeobecné symptomy, jako jsou bolest, nauzea či únava.
Zegarra a kol. ve své práci porovnávají finanční náklady na léčbu pacienta v režimu ambulantní chirurgie s pacientem, u kterého je nutný pobyt na lůžku po dobu první noci. U pacienta propuštěného bez nutnosti setrvání na lůžku udává až 35% redukci ceny (12 000$). Arregui a kol. udávají rozdíl v ceně 501 $ mezi ambulantně léčeným nemocným a pacientem s 23-hodinovou observací na lůžku. Farha a kol. udávají průměrnou cenu na pacienta operovaného v centru ambulantní chirurgie 2300 $ oproti 6500 $ vynaložených průměrně na laparoskopicky operovaného v sousední všeobecné nemocnici.
Závěr
Laparoskopická cholecystektomie může být provedena bezpečně u selektované skupiny pacientů zařazených do systému ambulantní chirurgie. Pacienti indikovaní k této léčbě však musí být důkladně vybráni a poučeni. Taktéž chirurg provádějící operaci musí mít dostatečné zkušenosti s laparoskopickými operacemi. Zajištění bezpečnosti operačního výkonu a dosažení dobrých výsledků nezávisí jen na chirurgicko-patologickém nálezu, ale i na individuálním přístupu, vhodné a precizní operační technice a plánované pooperační analgetické léčbě a na velmi úzké spolupráci Centra jednodenní chirurgie se systémem Home Care péče.
2.9 Literatura
- Arregui ME, Navarrete JL, Davis CJ, Hammond JC, Barkeu J. The Evolving Role of ERCP and Laparoscopic Common Bile Duct. Exploration in the Era of Laparoscopic Cholecystectomy. Int Surg. 1994;79:188–194.
- Baigrie RJ, Krahenbuhl L, Dowling BL. Laparoscopic Cholangiography through the gallbladder. J Am Coll Surg. 1994;178:175–176.
- Cushieri A, Dubois F, Mouiel J, Mouret P. The European Experience with Laparoscopic Cholecystectomy. Am J Surg. 1991;161:385–387.
- Czudek S, Kubiczek J, Branný J. Laparoskopická cholecystektomie a choledocholithiasa. Rozhl Chir. 1993;72(3):103–105.
- Czudek S. Jednodenní chirurgie. Praha: Grada;2009.
- Duda M, Czudek S, editoři. Mininvazivní chirurgie. Třinec: Nemocnice Podlesí; 1996.
- Duda M, Gryga A, Dlouhý M, Švach I, Mocňáková M. Nová éra léčby cholelithiasy. Čs Slov Gastroent. 1996;50(5):161–165.
- Dostalík J, Květenský M, Martínek L, Mrázek T.První zkušenosti s laparoskopickou cholecystektomií. Rozhl Chir. 1992;71:373–377.
- Niederle B. Chirurgie žlučových cest. Praha: Avicenum; 1977, s. 794.
- Paťha J, Louda V, Krbec J. Naše první zkušenosti s laparoskopickou cholecystektomií. Rozhl Chir.1992;71:378–381.
- Procházka V, Konečný M, Král, V, Duda M, Fialová J. ERCP v diagnostice a léčbě biliárních komplikací laparoskopické cholecystektomie. Čes SlovGastroent. 1999;53(5):140–144.